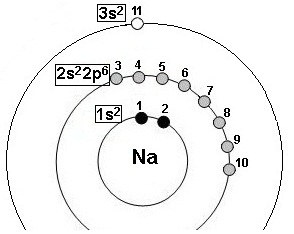
Énergie d’ionisation de l’atome de Sodium :
1- c'est le 11ème élément : Z = 11
2- structure électronique : 1s22s22p63s1 (voir classification)
3- groupes selon Slater : (1s2)(2s22p6)(3s1)
4- dessin correspondant

5- Énergie électronique totale du Sodium :
Etotale (Na) = 2E1+ 8E3+ E11
6- Énergie électronique de l'ion Sodium :
Etotale (Na+) = 2E1+ 8E3
7- I1 = Etotale (Na+) - Etotale (Na) soit I1 = - E11 (fin de l'exercice 2)
Z11= 11 – (8x0,35) – (2x1) = 2,2
I1 = - Ee11= - (2,22 / 32) x (- 13,6 eV) = 7,3 eV
 On a vu dans l'exercice précédent que la première énergie d'ionisation est égale à :
- E(dernier électron)
On a vu dans l'exercice précédent que la première énergie d'ionisation est égale à :
- E(dernier électron)
pour les éléments qui ne contiennent qu'un électron dans le dernier groupe de Slater
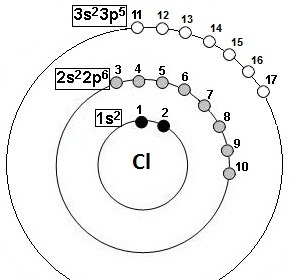
Energie d’ionisation de l’atome de Chlore :
1- c'est le 17ème élément : Z = 17
2- structure électronique : 1s22s22p6 3s23p5
3- groupes selon Slater : (1s2)(2s22p 6)(3s23p5)
4- dessin correspondant
5- Énergie électronique totale du Chlore :
Etotale(Cl) = 2E1 + 8E3+ 7E11
6- Énergie électronique totale de l'ion Chlore:
Etotale(Cl+) = 2E1 + 8E3+ 6E'11
voir l'exercice 1 avant de poursuivre ...
Correction complète ne cliquer que si les indications ne vous permettent pas de répondre à la question posée
Pensez à vérifier vos acquis et cochez les cases
![]() à la première page lorsque vous vous sentez capable de répondre à la requête proposée.
à la première page lorsque vous vous sentez capable de répondre à la requête proposée.