| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne
Devoir 1 : chimie inorganique descriptive
Correction du devoir 1 : Exercice1 ...
On vous propose, pour chaque question, un début de réponse pour vous aider.
1- Structure électronique des atomes.
a- Ecrire la configuration électronique complète et donner la représentation par les cases quantiques du Baryum (56ème élément) que l'on note (Xe) 6s2, puis
donner les nombres quantiques (préciser leur nom et leur fonction) du 46ème électron par ordre de remplissage.
Préciser sous chaque électron le chiffre donnant l'ordre de remplissage.
a- Le Baryum (56ème élément) que l'on note : (Xe) 6s2 = 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s2
1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 6s2
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ |
Le 46ème électron ... n = 4 l = 2
m = 0
s = -½
c'est à vous de continuer ...
b- L'élément Ag (47ème élément) que l'on note (Kr) 4d10 5s1, à partir de sa configuration électronique, expliquer pourquoi il est une exception à la règle de
Klechkowski (détaillez la règle de Klechkowski avant de l'utiliser dans vos explications).
b- Ag (47ème élément) que l'on note (Kr) 4d10 5s1 est une exception à la règle de Klechkowski.
Tout d'abord, que dit la règle de Klechkowski ?
Le remplissage des sous couche s'effectue dans l'ordre d'énergie croissant, celui-ci étant proportionnel à ...
... il stabilise la sous couche d en la complétant par ...
c'est à vous de continuer ...
c- Donner la configuration électronique de Fe, puis des ions Fe2+ et Fe3+. Pourquoi Fe3+ est-il l'ion le plus stable ?
c- La configuration électronique du fer : Fe = (Ar) 3d6 4s2 = 1s2 2s2 2p6 3s2 3p6 3d6 4s2
L'ion Fe+ = 1s2 2s2 2p6 3s2 3p6 ... L'ion Fe3+ = 1s2 2s2 2p6 3s2 3p6 ...
C'est l'ion le plus stable, c'est celui qui présente le plus de ...
c'est à vous de continuer ...
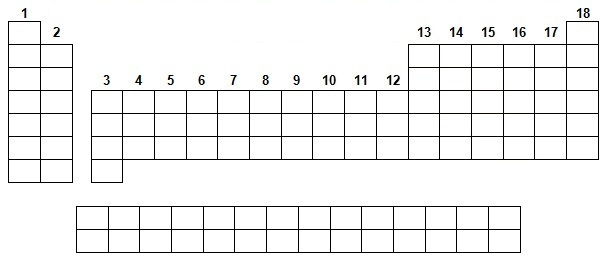
d- Colorer le niveau 5 (5s 5p 5d 5f) qui se répartit dans plusieurs périodes de la classification et utiliser la règle de Klechkowski (décrite précédemment) pour
expliquer ce décalage niveau / période.
|
d- Pour expliquer ce décalage niveau / période sur la classification, le niveau 5 est coloré et il se répartit dans les périodes : - 5 pour les sous couche s et p - 6 pour la sous couche d - 7 pour la sous couche f En effet, Klechkowski conduit à l'ordre de remplissage : 1s 2s 2p 3s 3p ...
que l'on peut découper en périodes :
c'est à vous de continuer ... |
 |
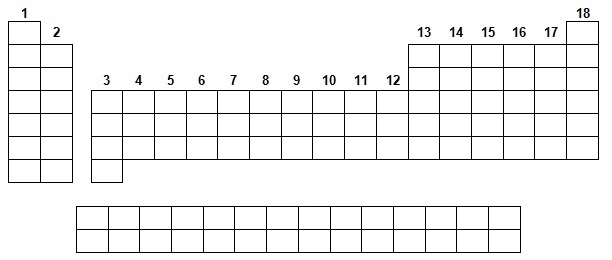
e- Utiliser la classification pour proposer les ions les plus probables en indiquant : +1, +2, +3, ... dans les cases.
Une seule réponse par case est demandé aussi proposer le plus probable. Commenter vos propositions.
e- Les ions les plus probables sont liés à la famille (colonne) à laquelle appartient l'élément :
| Les colonnes 1 à 7 conduisent logiquement aux ions de charge +1 à +7 par perte de tous les électrons de la couche de valence. Les colonnes 17 à 15 conduisent aux ions ... Les colonnes 13 et 14 conduisent respectivement aux ions ... Les colonnes 11 et 12 conduisent respectivement aux ions ... Enfin le bloc f donne les ions indiqués, ils vident ... |
 |
On peut proposer quelques ions supplémentaires concernant les éléments qui ...
Pour les éléments restant, des considérations particulières permettent d'expliquer les ions auxquels ils conduisent, comme le doublet
inerte (voir cours), comme les couches semi pleines, ... reste quelques ions ...
c'est à vous de continuer ...
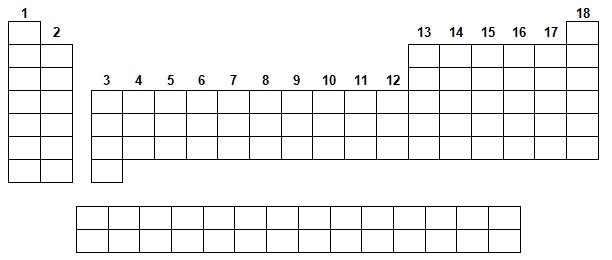
f- Placer les symbolisations IA, IB, IIA, IIB et expliquer leur positionnement.
f- Les symbolisations IA, IIA, ... sont d'anciennes normes
|
Les
colonnes 1, 2, 13 à 18 ont été numérotées de I à VIII et la lettre A (ou B selon le continent) a été accolée.
Les colonnes :
c'est à vous de continuer ... |
 |
Pour plus de détails cliquer sur la première ligne de correction mais seulement si vous ne trouvez pas !
| Pr Robert Valls | robert.valls@univ-amu.fr |