| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne
Devoir 1 : chimie inorganique descriptive
Correction du devoir 1 : Exercice 1 - Question e ...
1- Structure électronique des atomes.
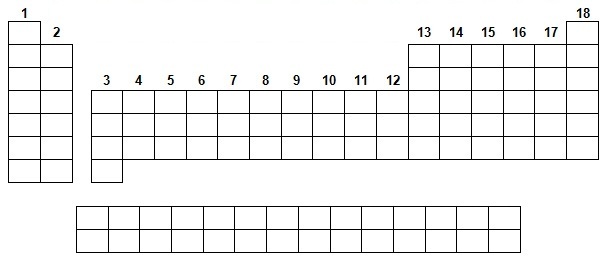
e- Utiliser la classification pour proposer les ions les plus probables en indiquant : +1, +2, +3, ... dans les cases.
Une seule réponse par case est demandé aussi proposer le plus probable. Commenter vos propositions.
e- Les ions les plus probables sont liés à la famille (colonne) à laquelle appartient l'élément :
| Les
colonnes 1 à 7 conduisent logiquement aux ions de charge +1 à +7 par perte de tous les électrons de la couche de valence.
Les
colonnes 17 à 15 conduisent aux ions Les colonnes 13 et 14 conduisent respectivement aux ions +3 et +4 pour les métaux (sauf la dernière période), ils vident leur sous couche s et p (de la couche de valence).
Les
colonnes 11 et 12 conduisent respectivement aux ions +1 et +2 (sauf Cu) |
 |
On peut proposer quelques
ions supplémentaires concernant les éléments qui perdent uniquement les électrons s sans modifier les
sous couche d (ou f). Pour les éléments restant, des considérations particulières permettent d'expliquer les ions auxquels ils
conduisent comme le
doublet inerte
(voir cours), comme les couches
semi pleines, ...
reste quelques anecdotes de la nature pour
lesquelles on trouve toujours des explications. En observant les réactivités, on constate, par exemple, que les
lanthanides donnent des ions +3 et une grande partie des actinides aussi.
Les composés du chrome III sont très stables, ainsi que ceux du cuivre II, du Neptunium, Osmium, Plutonium, Platine, Ruthénium IV ou
Palladium II et ainsi on
complète le tableau (le Mendélévium est très peu connu et les Rhodium et Iridium sont très stables, Ir étant le plus résistant des
métaux à la corrosion).
| Pr Robert Valls | robert.valls@univ-amu.fr |