| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne

ÉTUDE DES FAMILLES D'ÉLÉMENTS : le bloc s
Connaissances ... décrire ... les caractéristiques des éléments de la première colonne ...
Les alcalins possèdent un seul électron de valence (dernier niveau : ns1) aussi, plutôt que de compléter leur couche électronique pour obtenir la structure du gaz rare suivant, ils perdent un électron pour obtenir la structure du gaz rare précédent.
Les alcalins sont des métaux mous dont le point de fusion est peu élevé et sont de bons conducteurs de l'électricité.
Les éléments de cette famille sont très réactifs, ils doivent être conservés dans de l'huile de paraffine car leur réaction avec l'air ou l'eau est
plus ou moins violente (sauf Li).
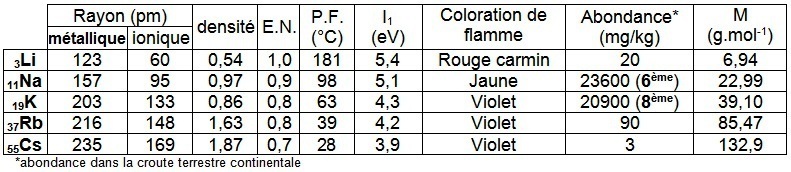
On observe les rayons atomiques les plus importants de chaque période de la classification, il en résulte une faible densité (0,54 à 1,87 alors que les éléments les plus denses sont à plus de 22).
Le rayon ionique est beaucoup plus petit que le rayon atomique car l’atome, lorsqu’il perd un électron, perd une couche électronique.
L’électronégativité est la plus faible de chaque période de la classification.
Ces corps fondent à basse température pour des métaux, jusqu'à 20°C pour Cs.
Les alcalins ont les plus faible valeur de I1 de la classification,
ce qui explique qu'ils soient surtout connus sous la forme ionique M+.
En effet, les ions Li+, Na+, ... ont la configuration électronique du gaz rare qui précède et sont
donc très stables.
Le sodium et le potassium sont relativement abondants dans la croûte terrestre et aussi dans les océans.
Etats naturels et obtentions
Les principaux minerais sont les suivants :
pour Li, il est extrait de divers aluminosilicates comme le spodumène LiAl(SiO3)2
pour Na, il est extrait de l’eau de mer ou de gisements de sel gemme
pour K, il est extrait de la sylvinite KCl,NaCl ou de la carnallite KCl,MgCl2
pour Rb et Cs, ils sont extraits en trace dans différents minerais
| pour Fr, il est à l’état de traces dans le minerais d'uranium | et il est formé par : | |
La réduction des alcalins est difficile et la seule méthode est la préparation par voie électrolytique des sels fondus (électrolyse ignée).
| Le Lithium est utilisé pour préparer le Tritium par bombardement de neutrons selon : |
Propriétés chimiques
Ce sont des métaux très réactifs :
• avec H2 vers 300°C, ils donnent les hydrures MH qui sont très réactifs du fait de la présence de H-.
• avec O2 on obtient les oxydes M2O.
• l’air fait fondre Li, ternit Na, K et Rb s’enflamment à chaud et Cs s’enflamme à 20°C.
• l’eau a une action lente sur Li, rapide sur Na et enflamme K, Rb et Cs.
Le I1 croît de Cs à Li aussi les électrons sont moins disponibles et l’élément est moins réactif.
| Pr Robert Valls | robert.valls@univ-amu.fr |