b- A partir du résultat précédent calculer la compacité sachant que RI = 175 pm.
c- A partir du résultat précédent calculer la compacité sachant que MI = 126,9 g.mol-1.
Devoir 2 : chimie du solide
 |
a- Montrer qu'il y a 8 atomes par maille. b- A partir du résultat précédent calculer la compacité sachant que RI = 175 pm. c- A partir du résultat précédent calculer la compacité sachant que MI = 126,9 g.mol-1. |
5- Cristaux moléculaires.
Le diiode cristallise dans un système
de type orthorhombique avec a = 978 b = 469
c = 714 en pm
Le volume de la maille est donné par :
a x b x c = 978 x 469 x 714 = 327498948 pm3
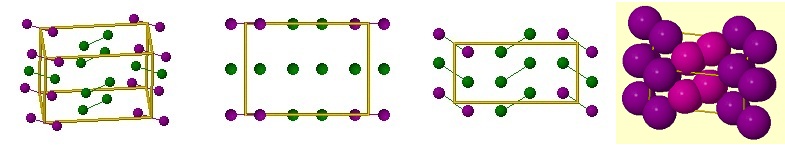
a- Si l'on considère la première vue, face la plus à gauche,
on constate que seul 2 atomes violets (flèches) sont
pour chacun à 50%
dans la maille (voir vue suivante), on compte donc (2
x 1/2) 1 atome violet.
On constate que seul un atome vert (entouré) est dans la maille. On
compte 1 atome vert.
Si l'on considère la première vue, le centre, on constate que seul 2
atomes (flèches) sont dans la maille.
On compte
50% des atomes du haut et du bas (flèches)
qui
comptent pour (
Par symétrie entre les deux faces la plus à gauche et la plus à droite on compte 1 atome violet et 1 atome vert.
Au total, il y a 1 + 1 + 2 + 2 + 1 + 1 = 8 atomes dans la maille
b- A partir du résultat précédent, on calcule le volume des 8 atomes :
8 (4/3 π RI3) = 8 [4/3 π (175)3]
= 179594380 pm3
compacité = volume des atomes / volume de la maille = 179594380 / 327498948 = 0,548
c- Sachant qu'il y a 8 atomes par maille, la masse volumique = masse des atomes / volume de la maille
masse volumique = (8 x 126,9
/ 6,02.1023) /
327498948.10-30
cm3 = 5,15 g.cm-3
Remarque : cette valeur est supérieure à la valeur mesurée car nous
avons considéré que les atomes sont des sphères or la dernière
vue
montre que dans la molécule I2 les sphères s'interpénètrent
(on considère que pour les sphères environ 4,3 % du volume est perdu).
Alors, on obtient : 5,15 x 0,957 = 4,93
g.cm-3 qui correspond bien à la valeur
mesurée.