Liaison ionique
La liaison ionique est le phénomène physique
qui lie les atomes entre eux par des forces
électrostatiques. Elle peut être
décrite, en simplifiant, par le fait qu'un ou plusieurs électrons sont
transférés d'un atome à un autre faisant qu'un des
atomes devient un ion positif et l'autre un ion négatif.
La liaison est donc due à une attraction électrostatique entre les ions formés et il n'y
a plus de paires d'atomes liés comme
pour la liaison covalente.

Les atomes sont liés par attraction coulombienne non-directionnelle qui concerne
un grand nombre d'atomes simultanément (les anions et les cations s'attirent
mutuellement dans toutes les directions de l'espace).
La liaison ionique pure n'existe pas et tous les composés présentent un degré
de liaison covalente.
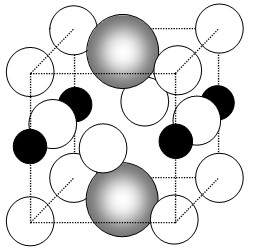
Les atomes s'empilent de différentes manières et on définit des volumes
élémentaires (comme celui proposé ci-contre) représentant l'ensemble de
l'empilement.
Dans cet exemple, il s'agit d'un cube contenant trois types d'ions (SrTiO
Atomistique et liaison chimique
La liaison chimique
![]()
Pr Robert Valls
robert.valls@univ-amu.fr