Energies d’ionisations de l’atome de Bore :
1- c'est le 5ème élément : Z = 5
2- structure électronique : 1s22s22p1 (voir classification)
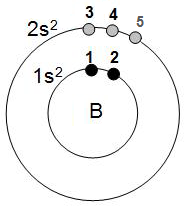
3- groupes selon Slater : (1s2)(2s22p1)
4- dessin correspondant

5- Énergie électronique totale du Bore :
Etotale(B) = Ee1 + Ee2 + Ee3 + Ee4 + Ee5 = 2 Ee1 +3 Ee3
Deux valeurs de Z à calculer car il y a 2 groupes de Slater
Ze1 = Z1
= Z2 = 5 – (1x0,3) = 4,7
Ze3 = Z3 = Z4 = Z5 = 5 – (2x0,35) – (2x0,85) = 2,6
Ee1 = E1 = E2
= (4,72 / 12) x E0 = - 300,4 eV
(E0 = - 13,6 eV)
Ee3 = E3 = E4 = (2,62 / 22)
x (- 13,6 eV) = - 23 eV
Etotale (B) = (2 x - 300,4) + (3 x - 23) =
- 669,8 eV
6- Énergie électronique totale de l'ion Bore : Etotale(B+) = Ee1 + Ee2 + Ee3 + Ee4 = 2 Ee1 + 2 E'e3
Deux valeurs de Z à calculer car il y a 2 groupes de Slater
Z1
= 5 – (1x0,3) = 4,7
Z'3 = 5 – (1x0,35) – (2x0,85) = 2,95
E1 = (4,72 / 12)
x (- 13,6 eV) = - 300,4 eV
E'3 = (2,952 / 22) x (- 13,6 eV)
= - 29,6 eV
Etotale (B+) = (2 x - 300,4) + (2 x - 29,6) = - 660 eV
7- I1 = Etotale (B+) - Etotale (B) soit I1 = (- 660) - (- 669,8) = 9,8 eV
Pensez à vérifier vos acquis et cochez les cases
![]() à la première page lorsque vous vous sentez capable de répondre à la requête proposée.
à la première page lorsque vous vous sentez capable de répondre à la requête proposée.