| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Chimie
inorganique
descriptive
Je consulte
des ressources
sur iut en ligne
Devoir 1 : chimie inorganique descriptive
Correction du devoir 1 : Exercice 3 ...
On vous propose, pour chaque question, un début de réponse pour vous aider.
3- Réactivité des éléments et nomenclature.
Les rayons atomiques
a- A l'aide du diagramme proposé, commenter les relations diagonales. Donner une explication aux différentes évolutions du rayon atomique selon les périodes
ou familles. Positionner dans chaque cas les éléments nécessaires aux commentaires.
b- En quoi les métalloïdes interviennent dans la notion de relation diagonale ?
c- Commenter l'évolution du rayon atomique lors du changement de période.
d- Les rayons atomiques varient de 1 à 10 alors que Z varie de 1 à 100. Commenter cette phrase.
| Les rayons atomiques b- Les métalloïdes interviennent pour étayer la notion de relation diagonale car ... c'est à vous de continuer ... |
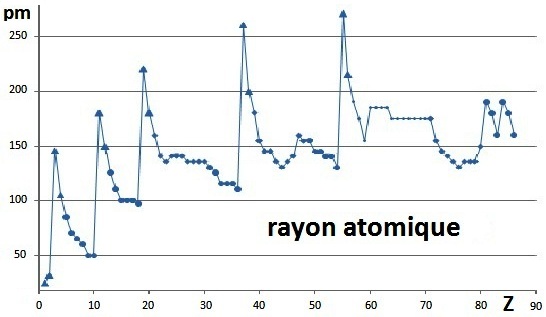 |
c- Lors du changement de période on observe une brutale augmentation du rayon atomique car ...
c'est à vous de continuer ...
d- Les rayons atomiques varient de 1 à 10 alors que Z varie de 1 à 100 car deux effets s'opposent ... c'est à vous de continuer ...
... lorsque l'on parcours la classification et si l'on passe du premier élément à 1 proton dans le noyau à l'uranium (dernier élément naturel)
à 92 protons dans le noyau soit un rapport de 92, les rayons atomiques ne varient que de 25 à 180 pm soit un rapport de 7.
Les ions et la nomenclature
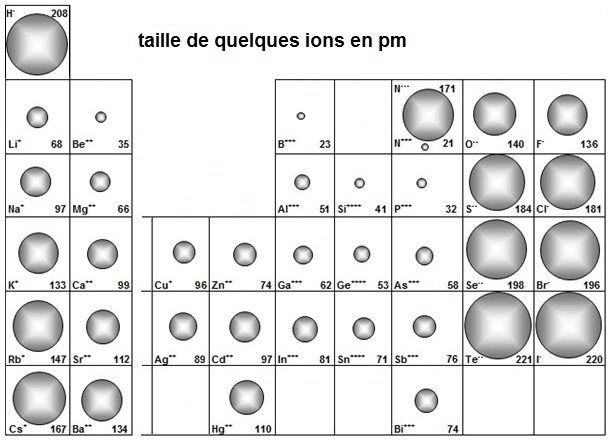
e- Commenter l'évolution des rayons ioniques par séries correctement choisies dans la figure proposée.
f- Nommer les ions suivants : HCO3-, S2O32-,
H3O+, HO-,
NH4+, CO32-, Na+, PO43-, Br-, Fe2+,
NO3-, SO42-, NO2-, S2-
Commenter les préfixes pour les deux premiers et les suffixes pour les quatre derniers.
g- Nommer les composés : H2, Cu, HI, MgO, H3PO4,
Fe2(SO4)3, CuNO2, (NH4)2CO3,
N2O3, H2S, K2SO3, FeS, Ca(OH)2 et donner leur formule
générale (et son nom).
h- Pour chacun des composés de la question c, préciser s'il s'agit d'un corps pur simple et/ou d'un corps pur composé, d'un atome, d'une molécule, d'un sel.
| Les ions et la nomenclature e- Les rayons ioniques de Li+ à Cs+ augmentent car dans une famille, à chaque période ... La série iso-électronique ... c'est à vous de continuer ... |
 |
| préfixe | |||
| HCO3- | ion | hydrogénocarbonate | "hydrogéno" ... |
| S2O32- | ion | thiosulfate | il s'agit de l'ion sulfate SO42- où ... |
| H3O+ | ion | hydronium | |
| HO- | ion | hydroxyde | |
| NH4+ | ion | ammonium | |
| CO32- | ion | carbonate | c'est à vous de continuer ... |
| PO43- | ion | phosphate | |
| Na+ | ion | sodium | |
| Br- | ion | bromure | |
| Fe2+ | ion | fer II | suffixe |
| NO3- | ion | nitrate | "ate" est utilisé pour la forme la plus ... |
| SO42- | ion | sulfate | "ate" est utilisé pour la forme la plus ... car il y a les sulfites ... |
| NO2- | ion | nitrite | "ite" est utilisé pour la forme la moins ... |
| S2- | ion | sulfure | "ure" est utilisé pour la forme qui compte le plus ... |
g & h- Nommer les composés suivants : H2, Cu, HI, MgO, H3PO4,
Fe2(SO4)3, CuNO2, (NH4)2CO3,
N2O3, H2S, K2SO3, FeS, Ca(OH)2
Préciser leur nature (corps pur simple et/ou corps pur composé
et/ou atome et/ou molécule et/ou sel). c'est à vous de continuer ...
| composé | formule | nom de la formule | nom du composé | corps pur simple | corps pur composé | atome | molécule | sel |
| H2 | ||||||||
| Cu | - | cuivre | X | X | ||||
| HI | ||||||||
| MgO | MO | oxyde métallique | oxyde de magnésium | X | X | |||
| H3PO4 | ||||||||
| Fe2(SO4)3 | MM'O | sel d'oxacide | sulfate de fer III | X | X | |||
| CuNO2 | MM'O | sel d'oxacide | nitrite de cuivre I | X | X | |||
| (NH4)2CO3 | ||||||||
| N2O3 | M'O | oxyde non métallique | sesquioxyde d'azote | X | X | |||
| H2S | ||||||||
| K2SO3 | MM'O | sel d'oxacide | sulfite de potassium | X | X | |||
| FeS | MM' | sel d'hydracide | sulfure de fer II | X | X | |||
| Ca(OH)2 |
Pour plus de détails cliquer sur la première ligne de correction mais seulement si vous ne trouvez pas !
| Pr Robert Valls | robert.valls@univ-amu.fr |