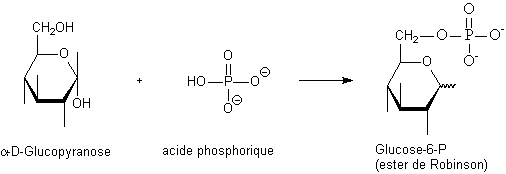
Les oses (monosaccharides)
Propriétés chimiques
Dues aux fonctions alcool
- H3PO4 (ac phosphorique):
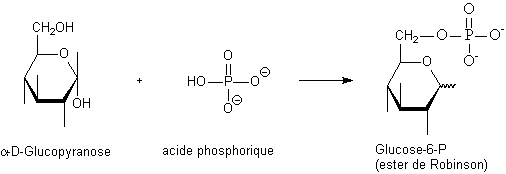
Intermédiaires indispensables du métabolisme (activation des oses) voir fig. 4.11
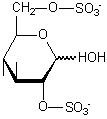
- H2SO4 (acide sulfurique)
esters sulfate: on les retrouve dans les:
- chondroïtine sulfate
- dermatane sulfate
- kératane sulfate
- héparine
Composants des polysaccharides acides du tissus conjonctif
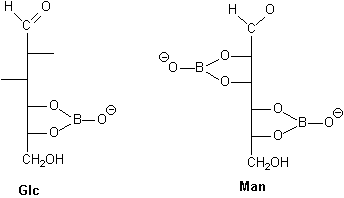
- H3BO3 (acide borique)
esters borates, suivant la position des -OH, on peut fixer 1 ou 2 borates, cela permet de ioniser les oses et ainsi de les séparer en fonction de leur charge (soit échange d'ions, soit électrophorèse)
- esters d'acides organiques: CH3-COOH (acide acétique)
esters acétiques (acétylation). Ils sont obtenus avec l'anhydride acétique. Si tous les -OH sont acétylés, on dit que le composé est peracétylé. L'OH hémiacétalique forme un pseudo ester facilement hydrolysable. Quand l’ose est engagé dans une liaison osidique il n’y a pas d’acétylation sur le –OH concerné (ni alcool, ni hémiacétalique).
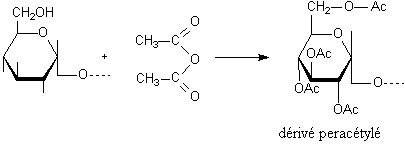
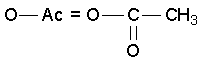
L’analyse des dérivés obtenus permet de déterminer les points de branchement des polyosides. Ces composés ne sont plus solubles dans l'eau, mais dans les solvants organiques. Ils sont stables à la chaleur , leur analyse sera effectuée en chromatographie en phase gazeuse)