| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne
Devoir 2 : chimie inorganique descriptive
Correction du devoir 2 : Exercice 1 - Question h ...
1- Etude des familles d'éléments : le bloc s
g- On propose la représentation de plusieurs molécules d'organomagnésien et on vous demande d'expliquer :
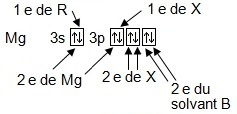
- au niveau électronique, la formation de cette structure, vous pouvez utiliser la représentation des cases quantiques pour étayer vos commentaires.
- les conditions pour que cette structure soit stable, vous pouvez compléter la représentation proposée.
h- Préciser le rôle et les caractéristiques du solvant
|
g- Il est proposé la représentation de plusieurs molécules d'organomagnésien qui sont disposées afin d'expliquer la formation du complexe par
l'interaction de trois complexes qui s'apportent mutuellement des
doublets dans des liaisons
de coordinance et la formation d’un
cycle à six atomes (type cyclohexane) où alternent liaisons σ et liaisons de coordinance ainsi qu'atomes de
Mg et atomes de X.
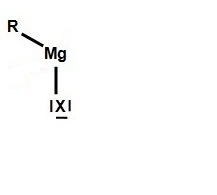
h- Le solvant B fournit, les
deux électrons manquant pour saturer la couche électronique, dans une autre liaison de coordinance et
il
stabilise alors l'organomagnésien (voir la première figure). |
|
| Pr Robert Valls | robert.valls@univ-amu.fr |