| Ressource d'IUT en ligne | Ressource d'IUT en ligneChimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne
Devoir 2 : chimie inorganique descriptive
(imprimer le sujet et compléter les pointillés et les tableaux proposées)
Correction du devoir 2 : Exercice 1 - Question a ...
1- Etude des familles d'éléments : le bloc s
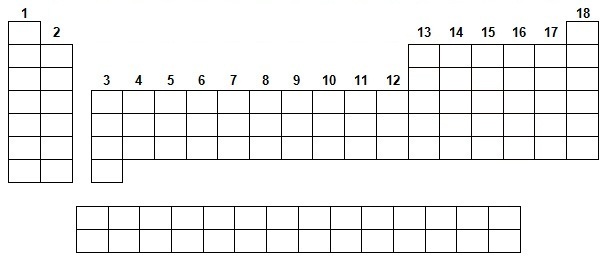
a- Positionner les familles du bloc s, en colorant les cases correspondantes de la classification proposée ci-contre et les nommer toujours sur la classification.
b- Décrire les familles du bloc s (attention : bien distinguer bloc et famille) en utilisant les différents rayons, l'électronégativité, le potentiel d'ionisation, les
réactivités vis à vis d'autres éléments et tout ce qui vous paraît caractéristique de ces familles.
|
a- On positionne les deux familles du bloc
b- Les alcalins possèdent un seul électron |
 |
Ce sont des métaux mous dont le point de fusion est peu élevé et ce sont de bons conducteurs de l'électricité.
Ils sont très réactifs et doivent être conservés à l'abri de l'air ou l'eau.
Avec H2 vers 300°C, ils donnent les hydrures MH qui sont très réactifs du fait de la présence de l'ion hydrure H-.
Avec O2 on obtient les oxydes M2O.
L’air fait fondre Li, ternit Na, K et Rb s’enflamment à chaud et Cs s’enflamme à 20°C.
L’eau a une action lente sur K, rapide sur Na et enflamme K, Rb et Cs.
Le potentiel de première ionisation (I1) croît de Cs à Li aussi les électrons sont moins disponibles et l’élément est moins réactif.
On observe les rayons atomiques les plus importants de chaque période de la classification, il en résulte une faible densité (0,5 à 2
alors que les éléments les plus denses ont des densité de plus de 22).
Le rayon ionique est beaucoup plus petit que le rayon atomique car l’atome, lorsqu’il perd un électron, perd une couche électronique.
L’électronégativité est la plus faible de chaque période de la classification.
Ces corps purs fondent à basse température pour des métaux, 20°C pour Cs.
La faible valeur de I1 permet par simple irradiation avec de la lumière, de faire émettre des électrons aux alcalins.
Les alcalino-terreux possèdent deux électrons de valence et donnent des ions M2+ très stables.
Pour la colonne 2, la réactivité est intense mais un peu moins que pour la colonne 1.
Les éléments de cette famille sont de bons conducteurs et prennent la forme d'un solide gris métallique plus dur que les alcalins.
Leur point de fusion est aussi plus élevé que celui des alcalins.
| Pr Robert Valls | robert.valls@univ-amu.fr |