| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Chimie
inorganique
descriptive
Je consulte
des ressources
sur iut en ligne
RÉACTIVITE DES FAMILLES D'ÉLÉMENTS
Correction de l'exercice :
La polarisabilité ...
a. Dans quel sens est dirigé le moment dipolaire α créé par deux charges + δ et
- δ, séparées par une distance d ?
a. Le sens du moment dipolaire est le même que celui du champ électrique, c’est-à-dire de
- δ vers + δ.
b. La polarisabilité a les dimensions d'un volume car elle peut s'exprimer en m3.
c.
C'est vrai, puisque toute molécule polaire (H2O) doit avoir un moment
dipolaire permanent sinon elle est apolaire (CH4).
d. Dans le cas de la molécule de CO2 le moment dipolaire est nul car c’est
toujours le cas pour ce type de molécules linéaires.
e. La molécule HCl a un moment dipolaire permanent et sa valeur en Debye est de
1,08.
En effet, la liaison O-H est
polarisée et conduit à deux moments dipolaires µOH qui donnent Contrairement à
la molécule de CO2, les deux moments ne s'annulent pas.
b. La polarisabilité a-t-elle les dimensions d'un volume ?
c. Une molécule polaire est-elle caractérisée par un moment dipolaire permanent ?
d. Le moment dipolaire d'une molécule de CO2 est-il nul ?
e. La molécule HCl a t'elle un moment dipolaire permanent ?
f. Une molécule d'eau est-elle polaire, du fait qu'elle possède un moment dipolaire permanent ?
on peut considérer cette molécule O=C=O comme la
juxtaposition de
deux dipôles égaux
et opposés selon : O→C←O
Le moment dipolaire résultant est la somme vectorielle des deux moments
dipolaire et elle est nulle.
f. La molécule d'eau possède un moment dipolaire permanent résultant de la somme
de deux
vecteurs selon le schéma proposé.
une
résultante µH2O.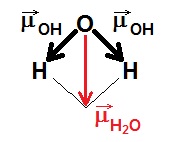
Pensez à revenir à la page "Connaissances
et compétences" pour vérifier vos acquisitions.
| Pr Robert Valls | robert.valls@univ-amu.fr |