| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne
J'envoie des commentaires
sur la ressource
RÉACTIVITE DES FAMILLES D'ÉLÉMENTS
Correction de l'exercice : Les rayons atomiques ...
Commenter la figure suivante en faisant des parallèles entre les deux types de graphiques :
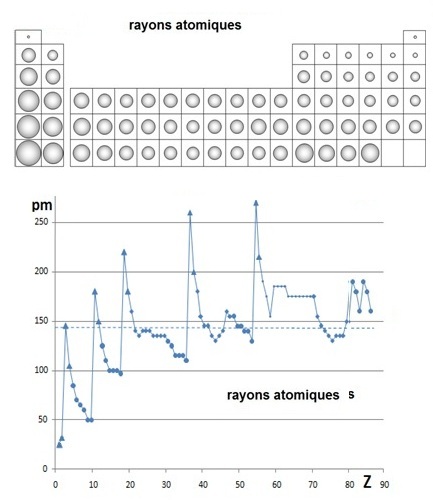 |
Le rayon atomique est un bon paramètre pour commenter les relations dans la classification :
-
relations horizontales et verticales Dans le premier car l'attraction du noyau dont le nombre de charge croît l'emporte sur l'augmentation de la répulsion entre les électrons dont le nombre suit la même évolution.
-
relations diagonales L'ensemble des relations est regroupé dans la figure et on a indiqué la famille des gaz rares. |
Pensez à revenir à la page "Connaissances et compétences" pour vérifier vos acquisitions.
| Pr Robert Valls | robert.valls@univ-amu.fr |