Chimie du solide: 1.3.3-2
Définir...
Influence des oxydes métalliques sur les propriétés des verres
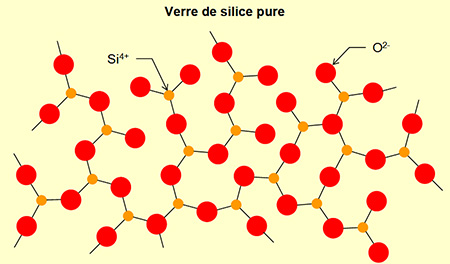
Le terme "verre" s'applique à tout solide amorphe présentant le phénomène de transition vitreuse. Donc de nombreux matériaux peuvent entrer dans cette catégorie : certains alliages métalliques, liquides moléculaires, polymères ... Ici nous ne parlerons que des verres "classiques" dont le constituant principal est la silice (SiO2). Cette silice est associée à d'autres oxydes, qui permettent d'abaisser sa température de fusion par formation d'eutectiques, et d'obtenir des propriétés physiques particulières. Les principaux oxydes utilisés sont : Na2O, BaO, CaO, Al2O3, B2O3, MgO, PbO. Dans la silice amorphe, les liaisons Si-O sont en partie covalentes et en partie ioniques, on dit qu'elles sont ionocovalentes. Les liaisons covalentes, qui sont des liaisons fortes, étant nombreuses (≈ 50 %), la température de fusion de la silice est élevée (> 1700 °C).
Un ajout modéré de métaux alcalins ou alcalino-terreux, qui ont une valence plus faible que le silicium (Si4+ : 4; Na+ : 1; Ca2+ : 2), conduit à la formation de liaisons Métal-O à caractère ionique plus marqué, donc moins fortes, ce qui fait baisser nettement la température de fusion. Par exemple, une liaison ionique Na-O, est environ 5 fois plus faible qu'une liaison ionocovalente Si-O.
Les verres les plus courants sont les sodocalciques de composition : SiO2 + Na2O + CaO + quelques additifs. L'oxyde de sodium permet d'abaisser la température de fusion et l'oxyde de calcium augmente la résistante chimique.
Influence de Na2O sur le verre de silice
Le diagramme simplifié du système binaire SiO2 - Na2O présenté figure ci-contre montre l'influence manifeste de l'oxyde de sodium sur la température de fusion du mélange.
Alors que la silice pure à une température de fusion voisine de 1745 °C, un mélange de silice avec 21 % en moles d'oxyde de sodium a une température de fusion d'environ 980 °C, soit une baisse de 765 °C.
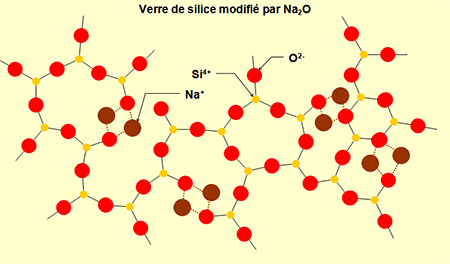
La présence du sodium va modifier le réseau aléatoire continu de la silice du verre. Les atomes de sodium pénètrent dans le réseau en "ouvrant" certaines mailles et se lient à des atomes d'oxygène. La liaison Na-O étant plus faible que la liaison Si-O, cela fait baisser la viscosité et la température de fusion (voir figure ci-dessous).
Les atomes d'oxygène apportés par Na2O vont eux s'intégrer au réseau, en se combinant aux atomes de silicium. Si le rapport molaire O / Si devient un peu trop fort (> 2,5), de nouvelles liaisons apparaissent dans le réseau qui devient alors plus rigide, et la solidification conduit à un produit cristallisé. Pour obtenir une structure vitreuse il faut donc utiliser des conditions particulières de refroidissement (vitesse très élevée).
Diagramme simplifié du système SiO2-Na2O
(partie qui nous intéresse ici)

Influence de Na2O sur la formation du verre de silice
(structures représentées uniquement en 2D)