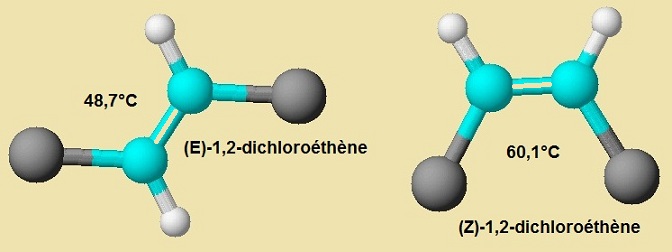
c- Les valeurs de températures d’ébullition sous une
atmosphère du (Z)-1,2-dichloroéthène et du
(E)-1,2-dichloroéthène
sont respectivement de 60,1°C et 48,7°C.

Comment interpréter ces valeurs expérimentales à l'aide des interactions de Keesom ?
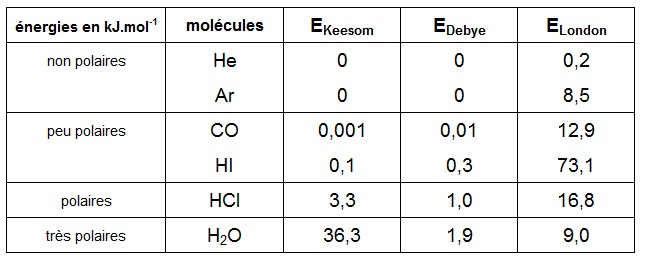
Plus le moment dipolaire sera grand plus les interactions seront fortes et plus
la température d'ébullition
du corps sera
élevée.
La molécule Z présentera le plus grand moment dipolaire car elle est
dissymétrique et sa température
d'ébullition sera plus
grande que pour la molécule E.
Pensez à vérifier vos acquis et cochez les cases
![]() à la première page lorsque vous vous sentez capable de répondre à la requête proposée.
à la première page lorsque vous vous sentez capable de répondre à la requête proposée.