DUT Chimie 11CG1
Correction de l'exercice : Deuxième principe - Définir ...
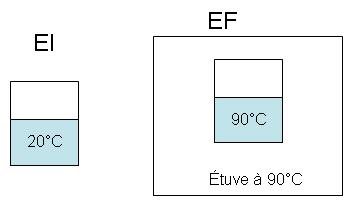
On chauffe un kilogramme d'eau de 20 à 90 °C au contact d'une atmosphère à 90 °C (un four à 90 °C).
Définir le milieu extérieur, le système et calculer ΔStotale,
ΔSextérieur et
ΔSsystème.
On rappelle que la chaleur spécifique de l’eau est ceau = 4,18 J.g-1.K-1.
Le système est le kilogramme d'eau, le milieu extérieur est l'étuve à 90 °C. En effet, l'eau se réchauffe
jusqu'à atteindre celle de la source d'énergie (l'étuve).
ΔSextérieur = Qextérieur /
Textérieur = 1000 x 4,18 x (90 -20) / 363 = + 806,1 J.K-1
ΔStotale = m . c . ln (Tf / Ti ) = 1000 x 4,18 x ln (363
/ 293) = + 895,5 J.K-1
On en déduit ΔSsystème = ΔStotale -
ΔSextérieur = 89,4 J.K-1
On ne donne pas de signe à la variation d'entropie du système car elle est toujours positive (ou nulle).
Pensez à revenir à la page
"Savoirs et savoir faire"
pour vérifier vos acquisitions.
Module 11CG1
Deuxième principe
L'entropie
Enoncé
Pr Robert Valls & Dr Richard Frèze
robert.valls@univ-cezanne.fr

