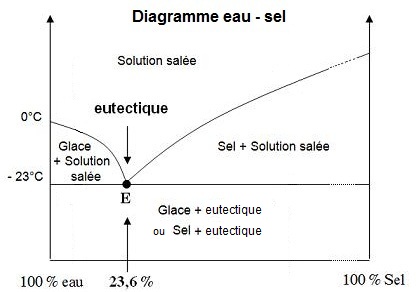
Les diagrammes d'équilibre solide-liquide peuvent aussi présenter un autre type
de minimum : ce sont des
diagrammes
à eutectique.
Il s'agit d'un diagramme simple de deux composés non miscibles.

Au point d'eutectie (E), la phase solide a la même
composition que la phase liquide et les courbes
solidus et
liquidus ont
le point E en commun.
Aussi, le mélange eutectique a le même comportement
qu’un corps pur.
L'eutectique est composé de 23,6 % de sel et de 76,4 %
d'eau et solidifie à - 23 °C et comme un corps pur,
il fond aussi à - 23 °C.
Remarque : le sel fond à plus de 800 °C, aussi le
diagramme n'est que partiellement représenté,
c'est ce qu'indiquent les pointillés.
L'étude de ce domaine n'aurait pas de sens dans ce
cours et dans l'exemple proposé.
On étudie le diagramme de part et d'autre du point E.
|
S’il y a beaucoup de sel sur la chaussée, lorsque la température baisse : - la solution salée de composition x refroidit jusqu’à A
- ensuite, du sel précipite (trait bleu) et la solution s’appauvrit en sel jusqu’à la composition de l’eutectique E
en suivant la courbe
du liquidus (trait
- à la température TE, tout se solidifie.
Globalement, on retrouve la composition x pour le solide (B) mais
microscopiquement il y a des cristaux de sel et des cristaux qui ont la
composition de l'eutectique. |
|
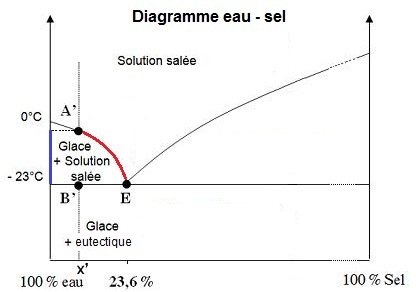
- la solution salée de composition x’ se refroidit jusqu’à A’
- ensuite, de la glace se forme (trait bleu) et la solution
- à la température TE, tout se solidifie. On peut utiliser
la règle du levier pour obtenir les
proportions de
Quelle que soit la composition initiale, on a donc un solide lorsque T est inférieur à - 23 °C :
- s'il y a beaucoup de sel au départ (chemin AB), on observe de gros cristaux de sel entourés de cristaux plus fins
- s'il y a peu de sel au départ (chemin A'B'), on observe de gros cristaux de glace entourés de cristaux plus fins
Les solides obtenus sont donc hétérogènes d’un point de vue microscopique.
 S’il y a peu de sel sur la chaussée, lorsque la température
S’il y a peu de sel sur la chaussée, lorsque la température
baisse :
s’enrichit en sel jusqu’à la composition de l’eutectique
en suivant la courbe
du liquidus (en rouge)
Globalement, on retrouve la composition x’ pour le solide
(B') mais microscopiquement il y a des cristaux de glace
et des cristaux qui ont la
composition de l'eutectique.
solution salée et de glace.
composé de 23,6 %
de sel et de 76,4 % d'eau (eutectique)
composé de 23,6 %
de sel et de 76,4 % d'eau (eutectique)
Cette partie de cours est principalement
constitués de connaissances, aussi vous devez la lire attentivement et la retenir.
Module 11CG1
Liquide - Solide
Pr Robert Valls & Dr Richard Frèze
robert.valls@univ-cezanne.fr