DUT Chimie 11CG1
Correction du devoir :
Thermodynamique I
I- Etude d’un changement d’état
Quelle est la quantité de chaleur nécessaire pour convertir 18 g de glace à -18 °C en vapeur à 100 °C
à pression atmosphérique ? (cglace = 2,1 J.g-1.K-1 ; Lfusion = 334 J.g-1 ;
Lvaporisation = 40,5 kJ.mol-1)
Il faut imaginer TOUTES les étapes pour passer de la glace à -18 °C à la vapeur d'eau à 100 °C.
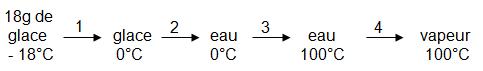
1 : Q1 = 2,1 x 18 x 18 = + 680,4 J
2 : Q2 = 334 x 18 = + 6012 J..................................
Q = Σ Qi = 54716,4 J
3 : Q3 = 4,18 x 18 x 100 = + 7524 J................74 % de l’énergie est consommée
4 : Q4 = 40500 x 1 = + 40500 J.........................
par la vaporisation de l’eau !
Module 11CG1
Enoncé Correction
Pr Robert Valls & Dr Richard Frèze
robert.valls@univ-cezanne.fr