On va construire des cycles utilisant des enthalpies de combustion, de formation et de liaison.
Exemple 1 : ....... ...........................1/2
N2 + 3/2 H2 → NH3
......................
avec ΔH à T = ?
c'est une enthalpie difficile à mesurer aussi on va utiliser les
enthalpies de combustion
pour
obtenir sa valeur.
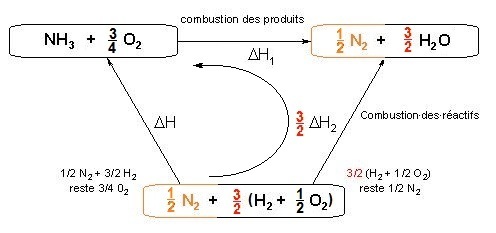
- combustion de l'ammoniac : .....NH3 + 3/4 O2 → 1/2 N2 + 3/2 OH2 .....avec ΔH1 à T = - 75,6 kcal.
- combustion du dihydrogène : .....H2 + 1/2 O2 → OH2 .............................avec ΔH2 à T = - 57,8 kcal.
- le diazote ne donne pas de combustion.
On construit un cycle (isotherme) qui va permettre de calculer la valeur de ΔH à T (en cliquant sur les liens dans l'ordre de lecture).
On place en haut du cycle la
réaction qui
contient le plus d'atomes.
Ensuite on utilise les autres
réactions
pour
lesquelles il faut ajouter
des atomes (colorés
en orange).
La dernière
réaction
est utilisée dans les
mêmes conditions.
On obtient le
cycle
attendu.
En cliquant sur la figure on
obtient la figure simplifiée.
On obtient : ΔH = 3/2 (- 57,8) - (- 75,6) = - 11,1 kcal
Les deux enthalpies de combustion et la construction du cycle, ont permis
d'obtenir l'enthalpie
difficile à mesurer.
Exemple 2 : On peut obtenir la valeur des enthalpies de
liaison de corps composés (ΔHC-H désigne
l'enthalpie de la liaison
entre C et H) à partir d'enthalpies de réaction
et de liaison (de corps simples).
C + 2 H2 → CH4
...........................
avec ΔHCH4 = - 75 kJ
(enthalpie de formation)
2 H (atomes libres)
→ H2
...................avec
ΔHH-H à T = - 435 kJ
(enthalpie de liaison)
C (atomes libres)
→ C
(graphite)....... .avec ΔHC
→ graphite ou
ΔHC à T = - 719 kJ
(enthalpie de liaison)
On peut écrire :
En utilisant la première réaction.
Puis la deuxième.
Enfin, la
troisième attention
au carbone qui s'écrit "C"
mais qui dans un cas est sous forme de graphite et
dans l'autre sous forme d'atome libre.
On obtient le cycle attendu.
En cliquant sur la figure on revient à la figure simplifiée.
ΔH2 = ΔH1 + ΔHCH4 =
(ΔHC
+ 2 ΔHH-H) + ΔHCH4
ΔH2 = [(- 719)
+ 2 x (-435)] + (- 75) = - 1664 kJ
ΔH2
= 4 ΔHC-H = - 1664 kJ
On obtient l'enthalpie cherchée : ΔHC-H = - 416 kJ