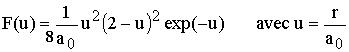
F(0.764) = 0.981 nm-1
F(5.236) = 3.610 nm-1
F(2) = 0 nm-1
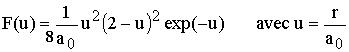 |
F(0.764) = 0.981 nm-1 F(5.236) = 3.610 nm-1 F(2) = 0 nm-1 |
Graphe de la fonction
| Orbitale 1s | Orbitale 2s | |
| Distance la plus probable (en u.a.) | 1 | 5.24 |
Une orbitale 2s a un rayon atomique 5 fois plus grand qu'une orbitale 1s. Un électron décrit par une orbitale 2s a une probabilité maximale de se trouver à une distance 5.24a0 du noyau alors qu'un électron décrit par une orbitale 1s a une probabilité maximale de se trouver à une distance a0 du noyau. Nous pouvons considérer qu'un électron 2s s'éloigne du noyau beaucoup plus qu'un électron 1s. Il pourra donc interagir avec d'autres atomes plus facilement qu'un électron 1s, participant ainsi à une éventuelle liaison chimique.