| Ressource d'IUT en ligne | Chimie Inorganique descriptive |

Je consulte
des ressources
sur iut en ligne

ÉTUDE DES FAMILLES D'ÉLÉMENTS : le bloc p
Connaissances ... nommer et situer ... la famille de l'azote ou colonne 15 ...
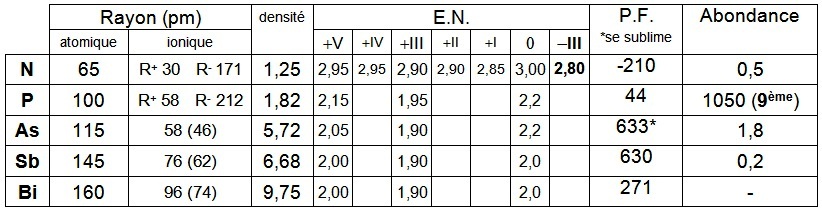
La famille de l'azote est formée de non métaux (N et P), de métalloïdes (As et Sb) et de métaux (Bi) généralement trivalents.
Le plus important est l'azote qui représente 80% de l'air.
Les propriétés de cette famille seront donc différentes.
N et P (blanc) sont des non métaux isolants ; P (noir) est semi conducteur comme As (jaune).
As (gris), Sb et Bi sont des métaux peu conducteurs. N donne un gaz de structure covalent moléculaire alors que P et As donnent des solides
qui présentent une structure covalente tétra-atomique (P4 et As4). Sb et Bi sont des solides métalliques.
Les éléments de la famille de l'azote possèdent cinq électrons de valence, ils peuvent donner des composés trivalents (N-IIIH3,
P+IIICl3,
N2+IIIO3, ...) ou pentavalents (P+VCl5) et on peut associer un D.O. mais
en principe, tous les dérivés sont covalents.
- D.O. +V ou +III : le caractère covalent est prédominant, car l'autre élément devrait avoir une électronégativité de 4 pour espérer avoir une liaison ionique.
- D.O. -III : le caractère ionique est possible avec N seulement s’il est combiné avec des éléments de χ ≤ 1,40 (alcalins et alcalino-terreux).
Acido-basicité des oxydes
On peut prévoir une évolution progressive du caractère acide à amphotère basique quand Z augmente (avec χ O-II = 3,50).
Ce sont des oxydes covalents indifférents ou exclusivement acides.
Les oxydes d'azote :
- N2O (DO +I) : protoxyde d'azote ou gaz hilarant (anesthésie).
- NO (DO +II) : monoxyde d'azote
- N2O3 (DO +III) : anhydride de l'acide nitreux HNO2.
- NO2 (DO +IV) : dioxyde d'azote = polluant automobile (pot catalytique).
- N2O5 (DO +V) : anhydride de l'acide nitrique HNO3.
Les oxydes de phosphore :
- P4O6 (DO +III) : anhydride de l'acide hypothétique phosphoreux H3PO3.
- P4O10 (DO +V) : anhydride de l'acide ortho-phosphorique H3PO4.
Les dérivés de l’hydrogène
On note que χH = χP donc hydrogène phosphoreux est plus adapté que phosphure d'hydrogène (P-III) ou hydrure de phosphore (H-I).
Dans tous les cas : Δχ est faible et les composés sont covalents aussi, on obtient les hydrures par voie indirecte.
Synthèse de l'ammoniac : N2 + 3 H2
![]() 2 NH3 (avec T = 550°C, P = 1000 atm, catalyseur -11 kcal/mol)
2 NH3 (avec T = 550°C, P = 1000 atm, catalyseur -11 kcal/mol)
Synthèse de l'homologue phosphoré : ¼ P4 + 3/2 H2
![]() PH3 (avec arc électrique +2,21 kcal/mole)
PH3 (avec arc électrique +2,21 kcal/mole)
Métaux : N et P donnent des combinaisons chimiques avec les métaux qui sont des nitrures (ioniques parfois covalents) ou phosphures (covalents). Beaucoup de nitrures sont de type insertion.
Quelques cas d'alliages métalliques (aciers cémentés Fe4N = très grande dureté).
Minerais : Le salpêtre (KNO3) est un minerai à mémoriser.
| Pr Robert Valls | robert.valls@univ-amu.fr |