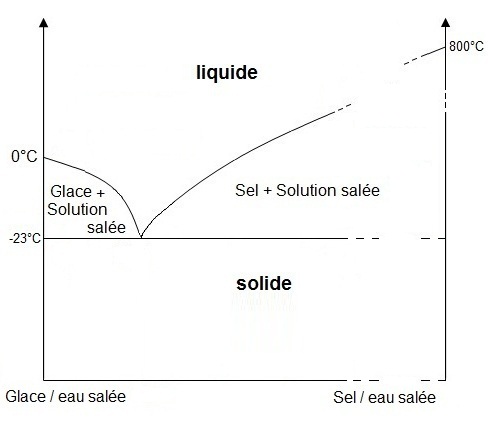
Au point eutectique (E) la phase solide a la même composition que la phase liquide et les courbes solidus et liquidus ont ce point en commun (le mélange eutectique a le même comportement qu’un corps pur).
S’il y a beaucoup de sel sur la chaussée, lorsque la température baisse :
- la solution salée de composition x
refroidit jusqu’à A
- ensuite, du sel
précipite et la solution s’appauvrit en sel jusqu’à la composition de l’eutectique (en suivant la courbe du liquidus)
- à la température
TE, tout se solidifie (on retrouve la composition x pour le solide).
S’il y a
peu de sel sur la chaussée, lorsque la température baisse :
- la solution salée de composition x’ se refroidit jusqu’à A’
- ensuite, de la glace se forme et la solution s’enrichit en sel jusqu’à la composition de l’eutectique (en suivant la courbe du liquidus).
Il se forme de la glace (ce qui pose problème pour la circulation
routière) bien qu’il reste du liquide.
A la température TE,
tout se solidifie (on retrouve la composition x’ pour le solide).