Les empilements les plus simples concernent les métaux puisque les atomes ont tous la même taille
et ne sont pas chargés
Les empilements les plus simples concernent les métaux puisque les atomes ont tous la même taille
et ne sont pas chargésélectriquement.
Les cristaux métalliques
sont constitués par une juxtaposition d’atomes identiques, liés par les forces électrostatiques de
Van der
Waals, aussi ces cristaux
métalliques sont en général malléables (peu durs).
On décrit le modèle du cristal parfait
,
en considérant
un
cristal sans aucun défaut et constitués
d'atomes identiques de rayon
parfaitement défini et qui sont
en contact.
Cependant, pour comprendre
ces empilements et pour visualiser leurs propriétés
géométriques, on les représente souvent comme
des petites
billes reliées par
des barres
matérialisant la maille.
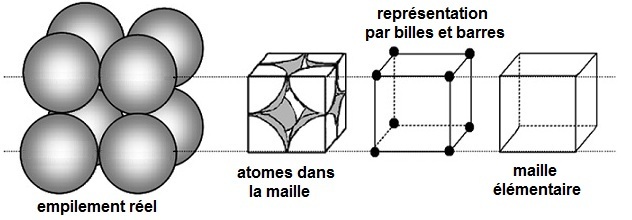
L'empilement le plus simple est cubique simple, il est représenté ci-dessous :
La maille ne contient que le
huitième de chaque atome donc 8 x 1/8 = 1 atome
(deuxième figure).
Chaque atome est en contact avec trois des atomes représentés (dans les trois
directions de
l'espace). Les sommets de la maille
élémentaire sont également les centres des
huit atomes.
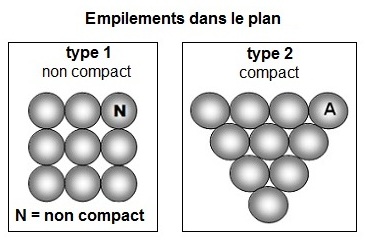 Ce n'est pas l'empilement le plus compact
Ce n'est pas l'empilement le plus compact
possible car, dans le plan on peut
imaginer
deux types
d'empilement :
- le type 1, que l'on qualifie de non compact
pour celui qui présente le plus
de vides
- le type 2, que l'on qualifie de compact
pour celui qui présente le moins de vides.
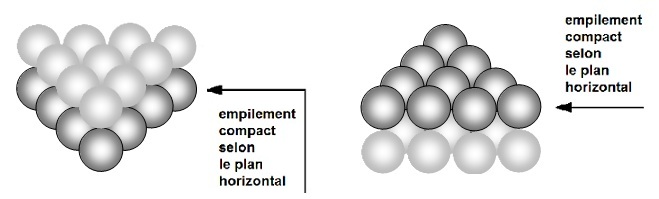
Plusieurs plans de type 1 ou 2 peuvent s'empiler
pour constituer un volume. Ils peuvent s'empiler
de façon non compacte et conduisent alors à la
première figure pour les type 1 et au volume
représenté ci-dessous pour le type 2.
Ce type d'empilement est peut courant mais permet de bien visualiser la notion
d'empilement
compact dans le plan (horizontalement)
ou
non compact
en volume (verticalement).
Associée à cette notion d'empilements, on propose la notion de coordinance. Il
s'agit du nombre de
voisins à égale distance et
les plus proches.
Dans l'empilement type 1, la coordinance
est de 6 car chaque atome est en contact avec un voisin à
droite
et à gauche, dessus
et dessous, devant et derrière soit 6 (selon les trois
axes).
Dans l'empilement type 2, la coordinance est de 8 car chaque atome est en
contact avec 6 voisin
dans le
plan (voir la figure) et
un dessus et un autre dessous, soit 8. Les autres
atomes ne sont plus
en contact et
on peut parler de coordinance d'ordre 2, 3, ...
en imaginant des sphères
concentriques
de plus en plus
grandes autour de l'atome considéré.
Chimie du solide Définition et étude des empilements Exercices
Pr Robert Valls & Richard Frèze robert.valls@univ-amu.fr